
Temă – Provocările etice și legale ale vaccinurilor si campaniilor de vaccinare
Lecții învățate în Japonia de la reacțiile adverse ale vaccinului HPV: o perspectivă a eticii medicale
Hirokuni Beppu, Masumi Minaguchi, Kiyoshi Uchide, Kunihiko Kumamoto, Masato Sekiguchi, Yukari Yaju
Indian Journal of Medical Ethics: https://doi.org/10.20529/IJME.2017.021
Abstract
Vaccinul împotriva virusului papiloma uman a fost corelat cu un număr de reacții adverse. Gama de simptome este una largă și se manifestă într-o manieră multistratificată pe o perioadă extinsă de timp. Argumentul pentru siguranța și eficacitatea vaccinului HPV omite următoarele neajunsuri: (i) fundația genetică a afecțiunilor autoimune nu este luată în considerare și argumentele ce ignoră acest fapt nu pot garanta siguranța vaccinului; (ii) mecanismele de evaziune imună ale HPV, ce necesită ca vaccinul HPV să mențină un nivel extraordinar de mare al anticorpilor pe o perioadă lungă de timp pentru a fi eficient sunt ignorate; și (iii) limitările eficienței vaccinului. De asemenea vom discuta problemele ce au apărut în cursul dezvoltării, promovării și distribuției vaccinului, precum și controversele întâlnite în monitorizarea cazurilor prezentînd reacții adverse și verificarea epidemiologică.
Introducere
În această lucrare, vom examina reacțiile adverse ca urmare a vaccinării împotriva virusului papilloma uman (HPV) în Japonia, și măsurile luate de către Ministerul Sănătății, Muncii și Bunăstării (MHLW) (1) de a retrage recomandarea activă a vaccinului. Aceste măsuri au provocat controverse domestice cât și internaționale. De asemenea vom discuta problemele ce au apărut în cursul dezvoltării, promovării și distribuției vaccinului; controversele întâlnite în monitorizarea cazurilor ce au prezentat reacții adverse și verificarea epidemiologică; precum și influența big pharma în politica din domeniul sănătății și cercetării.
I Prezentarea controversei vaccinului HPV în Japonia
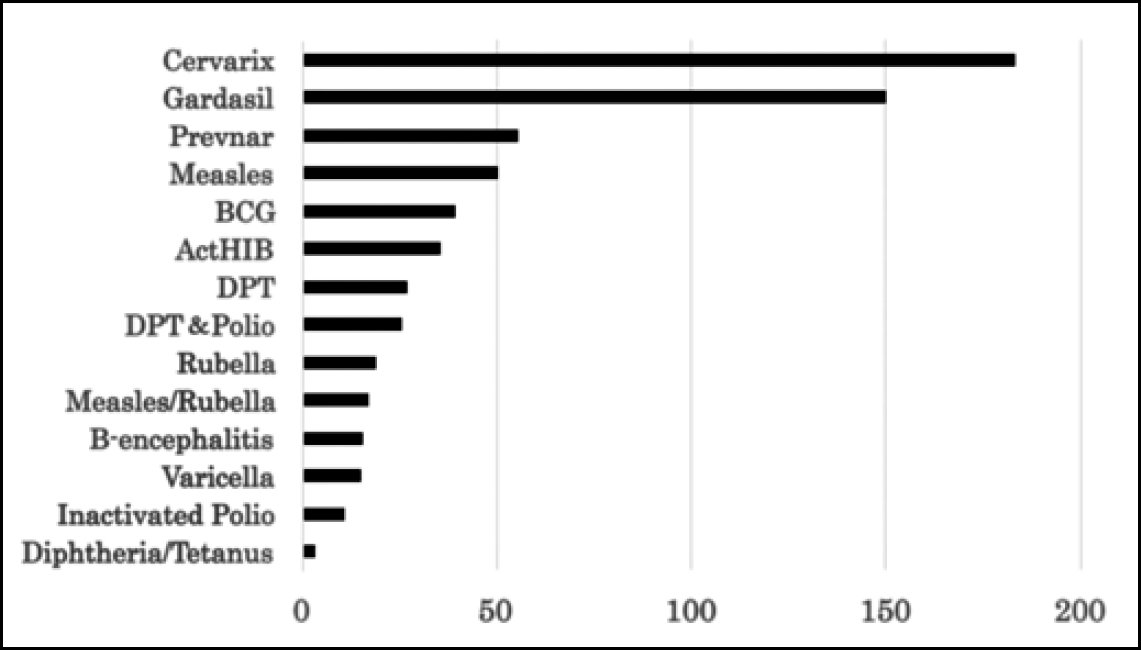
Vaccinurile HPV au fost aprobate mai târziu în Japonia decât în țările occidentale (Octombrie 2009 pentru Cervarix, și Iulie 2011 pentru Gardasil). Rata vaccinării a fost inițial scăzută. Totuși, după o campanie de promovare a vaccinului, ce a dus la o subvenție a vaccinului in Noiembrie 2010, rata a crescut exponențial. Acest fapt a fost urmat de o creștere neașteptată a efectelor adverse. Tabelul 1 prezintă numărul de efecte adverse serioase, definite în conformitate cu ghidurile ICH E2A (2), raportate de către producătorii de vaccinuri și medici la sfârșitul lunii Februarie 2016 (3). Numărul acestor cazuri depășește cu mult pe cel al altor vaccinuri, chiar și dacă este luată în considerare ipoteza că se acordă o atenție mai ridicată pentru vaccinuri nou introduse (4, 5) (Fig. 1). Din moment ce aceste date au fost alcătuite din declarații voluntare, incidența reală a efectelor adverse ar putea fi mai ridicată (6, 7).

Alte aspecte cheie ale reacțiilor averse declarate ale vaccinurilor HPV consistă în diversitatea simptomelor și dezvoltarea într-o manieră multistratificată pe o perioadă extinsă de timp. Efectele adverse includ simptome multisistematice complexe, precum atacuri de apoplexie, tulburări ale conștiinței; durere cronică incluzând migrene, mialgie, artralgie, durere de spate și de alte feluri; disfuncții motorii, precum paralizie, slăbiciune musculară; oboseală și mișcări involuntare, amorțeală și tulburări senzoriale; simptome autonome, precum amețeală, hipotensiune, tahicardie, greață, vomitare și diaree; disfuncții respiratorii, incluzând dispnee și astm; tulburări endocrine, precum tulburări menstruale și hipermenoree; hipersensibilitate la lumină și zgomote; simptome psihologice, precum anxietatea, frustrarea, halucinarea și mâncatul excesiv; disfuncții cerebrale și deficite cognitive, inclusiv pierderea memoriei, dezorientare și pierederea puterii de concentrare; și turburări de somn, incluzând hipersomnia și narcolepsia. În anumite cazuri, aceste simptome afectează învățarea și rezultă în oboseală excesivă și pierderea motivației, având un efect negativ asupra vieții de zi cu zi (8, 9, 10, 11). Situația în Japonia este similară cu cea a altor țări ce au raportat de asemenea o gamă specifică de simptome severe și complexe ce se manifestă pe o perioadă extinsă de timp (12, 13).
Motivul pentru care vaccinurile HPV provoacă aceste efecte adverse caracteristice rămâne a fi studiat în viitor, dar una din explicațiile plauzibile este că aceste vaccinuri sunt dezvoltate pentru a menține un nivel de anticorpi extrem de ridicat pe o perioadă lungă de timp. Din moment ce reacțiile inflamatorii asociate cu infecția sunt cunoscute a cauza afecțiuni autoimune și deteriorarea reacțiilor autoimune (14); stimularea antigen a vaccinurilor HPV poate induce reacții autoimune printr-un mecanism similar cu cel al infecțiilor prelungite.
Persoanele care au avut parte de efecte adverse ca urmare a vaccinării HPV au instituit o asociație cu scopul de a facilita comunicarea cu alte persoane care au avut de suferit în Japonia. Atunci când aceste efecte adverse au fost reflectate în mass-media, vaccinarea HPV a devenit o problemă socială majoră. În răspuns la presa negativă în privința vaccinării, MHLW a retras recomandarea activă in iunie 2013 pe motiv că “s-a stabilit o relație de cauzalitate între vaccinare și afecțiunile adverse” (1). Ca urmare, rata inoculării a scăzut drastic [de la maximul de 80% la 1% în prezent (15)]. În răspuns la această evoluție, adepții vaccinului HPV au inițiat o campanie în sens contrar și au început activități de lobbying către guvern.
În 20 Ianuarie 2014, comitetul consultativ înființat de MHLW (16) și-a prezentat punctul de vedere că durerile și afecțiunile motorii prezentate de multe persoane în urma vaccinării HPV cuprind reacții psihosomatice la anxietate sau durere stimulatorie cauzată de injecție, și nu sunt datorate de componentele vaccinului în sine. Însa doctorii și cercetătorii care au examinat pacienți cu simptome post-vaccinatorii au ajuns la o altă concluzie, evidențiind simptomele caracteristice și evoluția acestora, ce nu pot fi ușor explicate ca reacții psihomatice (9, 10, 11).
Astfel, siguranța vaccinului HPV rămâne incertă în Japonia, justificând neîncrederea publică. Recunoscând influența potențial negativă asupra opiniei publice în alte țări, companiile farmaceutice au lansat o campanie contra-intervențională prin organizații publice și private, precum Organizația Mondială a Sănătații. Comitetul Consultativ Global pentru Siguranța Vaccinurilor (GACVS), unul dintre comitetele OMS, a declarat că
“nu a descoperit probleme de siguranță ce îi permit alterarea recomandării în privința utilizării vaccinului” și a criticat decizia MHLW de a-și retrage recomandarea activă (17).
În ciuda acestor obstacole, o asociație a victimelor a intentat un proces in Curțile Districtuale Tokyo, Nagoya, Osaka și Fukoka împotriva guvernului și a celor două companii farmaceutice ce au produs aceste vaccinuri. În plus, mai multe victime s-au alăturat procesului, crescând numărul complet al reclamanților la 119 (18).
Până acum, am revizuit reacțiile adverse la vaccinul HPV și măsurile luate de MHLW în Japonia ce au provocat controverse la nivel național cât și internațional. În secțiunea următoare, vom discuta siguranța și eficacitatea vaccinurilor HPV promovate de OMS și alte organizații, și vom identifica erorile în premiza argumentelor în favoarea vaccinurilor.
II Problema cu vaccinul HPV: refutarea declarației GACVS (19)
a. Probleme de siguranță
Investigația MHLW
În privința Japoniei, declarația GACVS (17) afirmă că
“verificarea datelor clinice de către comitetul național a dus la concluzia că simptomele nu au fost corelate cu vaccinul”.
În ciuda acestui fapt sunt carențe majore în investigația comitetului (16).
Problema cea mai serioasă este că foarte puțini membri au consultat personal pacienți cu simptome post-vaccinatorii. Investigația comitetului se bazează exclusiv pe durere și tulburări motorii, și ignoră multe alte simptome ce au fost observate. Mai mult, cazurile în care efectele adverse s-au petrecut cu mai mult de o lună după vaccinare au fost excluse din considerente cum ar fi că majoritatea efectelor vaccinării se petrec în prima lună după vaccinare. Totuși, studiile ulterioare au clarificat că simptomele pot apărea după o perioadă semnificativă de timp după vaccinare (9, 10, 11).
Metodele utilizate în determinarea reacțiilor psihosomatice drept cauzele simptomelor rămân în discuție de asemenea (16). Comitetul consultativ a propus patru ipoteze în legătură cu patofiziologia simptomelor post-vaccinatorii: (i) tulburări neurologice, (ii) intoxicație, (iii) reacție imunologică și (iv) reacție psihosomatică. Cazurile ce nu sunt în concordanță cu criteriile comitetului pentru (i)-(iii) au fost considerate ca neavând o legătură de cauzalitate cu vaccinul HPV. Totuși din moment ce definiția răspunsului psihosomatic este ambiguă și diagnosticul este determinat exclusiv de opinia subiectivă a medicului, multe cazuri au fost diagnosticate ca reacții psihosomatice.
Susținerea concluziei comitetului consultativ nu este nicidecum universală. Doctori și cercetători care au examinat pacienți cu simptome post-vaccinatorii au susținut că este dificil de caracterizat toate simptomele ca fiind reacții psihosomatice pe baza rezultatelor experimentelor și raportărilor (8, 9, 10, 11, 20, 21, 22). Înaintea investigației neuro-imunopatiei (HANS) asociată cu vaccinul HPV, un nou concept patologic propus de Nishioka (22), Yotoka et al a exclus din studiu toți indivizii care au prezentat orice anomalie fizică sau pshică înaintea vaccinării (9). Astfel, structura studiului întărește concluzia că răspunsul psihomatic nu poate justifica majoritatea efectelor adverse, precum susține comitetul.
În plus, din moment ce 11 din 15 membri ai comitetului consultativ au parte de conflicte de interese cu producătorii vaccinului, publicul este justificat să solicite ca o gamă mai variată de cercetători să revizuiască datele relevante (23). Astfel, siguranța vaccinului HPV rămâne incertă în Japonia, justificând îndoielile publicului. În afara Japoniei, Jefferson et al (24) și Gõtzsche et al (25) de asemenea și-au exprimat îngrijorarea în legatură cu natura și calitatea reglementării vaccinului HPV de către Agenția Europeană a Medicamentului.
i. Criticarea justificării siguranței menționata în declarația GACVS
În privința siguranței vaccinului HPV, GACVS susține în declarația sa că nu a descoperit nicio problemă necesitând alterarea recomandării sale pentru utilizarea vaccinului, și a criticat Japonia pentru că a sistat promovarea activă a vaccinului HPV (17). Totuși, studiile (26, 27, 28, 29, 30, 31) citate de GACVS ca dovadă a siguranței vaccinului ridică următoarele întrebări.
ii. Fundația genetică a autoimunității
Printre mecanismele patofiziologice legate de reacțiile adverse ale vaccinării, implicarea autoimunității este cea mai probabilă. Mecanismele diverse sugerate in privința afecțiunilor autoimune includ: mimetismul molecular (32), în care un antigen străin împărtășește o similitudine structurală cu un auto-antigen; disruperea mecanismelor esențiale in toleranța imunitară centrală și periferică (33); și retrovirusurile endogene umane producând proteine funcționale sau anticorpi împotriva proteinelor proprii (34).
Deși etiologia nu a fost complet elucidată, majoritatea afecțiunilor autoimune constituie stări poligenice complexe, prin care individul afectat succede polimorfisme genetice multiple ce contribuie la succetibilitate pentru boli, iar aceste gene interacționează cu factorii de mediu pentru a cauza afecțiunea. Este un fapt bine-cunoscut că unele alele ale leucocitelor antigen se produc la o frecvența mai înaltă la pacienții cu anumite afecțiuni autoimune decât în populația generală (35).
În prezent, ce se presupune a fi dovada principală cu privire la siguranța vaccinului HPV este aceea că nu există o diferență statistică semnificativă între incidența afecțiunilor autoimune între femeile vaccinate și cele nevaccinate sau restul populației. Totuși, din moment ce proporția populației succeptibile genetic față de restul populației este foarte limitată, comparația între incidența afecțiunilor autoimune între cei ce au fost vaccinați și grupul de control (nevaccinat) nu este probabil să exprime o diferență semnificativă. Argumentele ce nu iau în considerare acest fapt nu pot asigura siguranța vaccinului. Răspândirea de bază a multor afecțiuni autoimune este relativ scăzută. Astfel, supravegherea atentă post-marketing pe scară largă ce ia în cont caracteristicile imunologice ale pacienților individuali este necesară pentru a verifica relația dintre vaccinare și afecțiunile autoimune (36).
iii. Codificarea și lipsa de informații prețioase
În agențiile de reglementare a medicamentelor și industria farmaceutică, toate reacțiile adverse din dosarul medical al pacientului sunt codificate pentru procesare digitală și astfel, detaliile conținute în datele neprelucrate sunt “pierdute”. Ca atare, significanța clinică și riscurile medicamentelor sunt mascate (37, 38). Acest proces rezultă într-un fel de raționament circular, prin care simptomele post-vaccinatorii sunt izolate și analizate retrospectiv în cadrul conceptelor patologice existente.
b. Schimbarea de paradigmă
HPV este echipat cu anumite mecanisme de evaziune imună, ce pot cauza sistemul imunitar să devină mai permisiv cu infecția, creând un micromediu succeptibil pentru alte infecții și facilitând neoplazia intraepitelială cervicală (CIN). Pentru a contracara aceste mecanisme de evaziune imună, vaccinul HPV este produs cu scopul de a menține un nivel extraordinar de mare al anticorpilor pentru cel puțin un deceniu (39, 40). Acest fapt elimină vaccinul HPV din paradigma “vaccinului” precum el este cunoscut conventioal. Aceste caracteristici unice ale vaccinului HPV duc la o evaluare mai aprofundată a siguraței sale să fie esențială.
c. Eficacitatea
Deși declarația GACVS susține că “impactul vaccinurilor HPV pe urmările clinice legate de HPV, inclusiv leziunile pre-tumorale, este bine stabilită”, în realitate, eficiența vaccinului HPV este destul de limitată, precum este ilustrat în cele ce urmează.
În primul rând, singurul efect observat al vaccinului HPV are un efect preventiv asupra leziunilor pre-tumorale (în mod specific CIN); efectul preventiv asupra cancerului cervical nu a fost demonstrat. Efectele vaccinurilor aprobate curent în Japonia (Cervarix și Gardasil) pe leziunile pre-tuomorale au fost demonstrate numai în cazurile virusurilor HPV 16 și respectiv 18, care în conformitate cu cele mai sigure studii, reprezintă doar 50% dintre cauzele de cancer cervical în Japonia (41).
Mai mult, maxim 10% dintre cazurile de infecție HPV cu risc înalt conduc la infecție persistentă ce poate cauza cancer, în timp ce marea majoritatea leziunilor pre-tumorale (CIN) se ameliorează înainte de a deveni maligne (42, 43). În acest caz, doar 0,15% dintre persoanele infectate cu HPV cu risc înalt pot ajunge la cancer (44, 45). Chiar cu apariția cancerului, vizitele medicale regulate îl pot detecta într-o fază incipientă și tratamentul corespunzător (operație, radioterapie sau chimioterapie) poate salva multe vieți. În baza acestor fapte, promovarea activității educaționale ce scoate în evidență importanța controalelor și a detecției timpurie, precum și crearea unui mediu în care femeile se simt mai comfortabil să urmeze testul Papanicolaou, ar fi mult mai eficient să prevină cancerul cervical decât constângerea fetelor să se supună vaccinării HPV prezente, cu toate lipsurile ei.
Adepții vaccinurilor HPV susțin că sunt până la 98%-100% eficiente în prevenția cancerului cervical. În realitate, totuși, reducerea de risc absolută (ARR) dată de vaccinurile HPV este de cel mult 0,1%-0,7%, pe baza calculărilor utilizând datele existente (46). (!)
Mai mult, aceasta indică numai reducerea riscului de leziui pre-tumorale, în timp ce riscul cancerului cervical rămâne necunoscut.
Promovarea controalelor medicale pentru cancerul cervical este o altă măsură împotriva canerului cervical. În ultima vreme, s-a acordat atenție ratei scăzute de control a cancerului cervical în Japonia în comparație cu țările occidentale. În special, tinerele ce nu au avut încă parte de sarcini ezită să se supună examinărilor ginecologice în Japonia. Accesul la examinări realizate de doctorițe și acceptarea prelevării mostrelor pe cont propriu ar crește fără îndoială rata controalelor. În fapt, promovarea controalelor pentru cancerul cervical a redus semnificativ incidența ajustată pe termen de vârstă a canerului cervical în Marea Britanie (47).
III. Defectele structurale: un punct de vedere al eticii
În secțiunile precedente, am discutat problemele variate legate de siguranța și eficacitatea vaccinului HPV. Este acum adecvat să discutăm cum astfel de vaccinuri dubioase au ajuns să fie larg răspândite.
Răspunsul, cel puțin cu privire la Japonia, poate fi găsit in defectul structural, în combinație specifică cu următorii factori: (i) promovarea agresivă de către industria farmaceutică, (ii) negocierile comerciale de către superputerile economice, și (iii) medicina contemporană, ce este caracterizată prin încrederea excesivă în tehnologie și lipsa modestiei cu privire la ascultarea doleanțelor pacienților.

a. Actul de Imunizare și promovarea vaccinului de către producători.
Urmând promulgării Actului de Imunizare în Japonia în 1948, numeroase procese au fost intentate în răspuns la lezări cauzate de vaccinuri. Acest fapt a rezultat în stabilirea unui sistem de compenare a victimelor și rectificarea legilor si reglementărilor relevante. În prezent, vaccinurile sunt împărțite in trei categorii, ilustrate în Tabelul 2 (48).
Conform cu definițiile din acest act, un vaccin pentru protecție individuală, precum vaccinul HPV, are trebui clasificat ca “opțional”, ce depinde exclusiv de alegerea individuală. Totuși, datorită activităților de lobbying, vaccinul HPV a fost aprobat ca un vaccin ce trebuie administrat din cheltuiala publică, și a fost inclus în categoria “Vaccinare de rutină de tip A”. Din moment ce a fost recomandat de către guvern, indivizii se simpt obligați să fie vaccinați.
Comisia Japoneză de Experți pentru Eradicarea Cancerului Cervical (49), una dintre cele mai puternice organizații de lobbying din Japonia, a fost fondată în Noiembrie 2008, în același timp în care vaccinul HPV era considerat pentru aprobare. Membrii executivi ai diverselor soceități academice s-au înscris în acest grup și au excercitat o influență considerabilă asupra procesului legislativ, precum și asupra administrației publice și conturarea opiniei publice.
În conformitate cu informațiile obținute de Medwatcher Japan (50) din Ghidul de Transparență în Relația dintre Activitățile Corporative și Instituțiile Medicale (51) al Asociației Producătorilor Farmaceutici din Japonia, fondurile obținute de Comisia de Experți de la producătorii de vaccinuri se acumulează la ¥73,500,000 (¥35,000,000 în 2012 și ¥38,500,000 în 2013). În plus, s-a relevat că secretarul Comisiei de Experți lucrează ca Director de Marketing pentru vaccinuri al GlaxoSmithKline Co. începând cu cel puțin opt luni înainte de lansarea Cervarix. Aceste fapte sugerează că activitatea Comisiei de Experți nu a fost nicidecum una altruistă, ci de fapt constituie o promovare mascată (52).
b. Presiunea exercitată din afara Japoniei
Promovarea vaccinului HPV în timpul negocierilor comerciale între Japonia și Statele Unite a creat de asemenea presiune în adoptarea vaccinului. Pentru mulți ani, promovarea vaccinărilor a fost una dintre cele mai insistente cerințe in negocierile comerciale cu Statele Unite (53, 54). Centrul pentru Studii Strategice și Internaționale, un think tank civil, parte a complexului militar-industrial al Statelor Unite, a criticat indecizia guvernului Japoniei în rapoartele eliberate în Mai 2014 și Aprilie 2015, reflectând iritarea industriei americane (55, 56).
c. Medici uitându-și rolul
Defecte intrinsece în comunitatea medicală fundamentează problema vaccinului HPV. În 2004 Sheldon Krimsky a remarcat că influența în creștere a comercialismului în știința academică și cercetarea biomedicală în cartea sa, Știința în interesul privat (57). A scris,
“… amestecul dintre știință și comerț continuă să erodeze standardele etice de cercetare și diminuează încrederea publică în rezultatele sale. ”
În cei 13 ani de la publicare, acest avertisment a ajuns realitate peste tot în lume. Inițial, sănătatea publică și farmaco-epidemilogia erau câmpurile științifice ce vizau protecția pacienților individuali și a publicului. Totuși, realitatea curentă diferă foarte mult față de acest ideal.
Știința este acum abuzată pentru a proteja interesele industriei farmaceutice, și a fost utilizată pentru a nega relația de cauzalitate între medicamente și reacțiile sale adverse. Mulți cercetători și experți încearcă să excludă adevărurile neconvenabile din considerare.
“Taxonomia bolilor reprezintă cel mai apropiat câmp de știință față de natură, dar rămâne o construcție teoretică. Este teoria aceea ce trebuie părăsită atunci când simptomele pacientului nu sunt în concordanță, nu relatarea pacientului asupra propriei sale experiențe.” (58, 59)
Aceasta înseamnă că doctorii trebuie să fie mai modești și onești. Diagnosticule și terapiile de astăzi au fost dezvoltate prin ascultarea vocilor pacienților și examinarea minuțioasă. Este iresponsabil a ignora plângerea pacientului ca o reacție psihogenică sau ca un fenomen general în lipsa unei analize amănunțite.
IV. Considerații întru rezolvarea problemelor
Precum s-a descris în secțiunea III, introducerea vaccinării HPV în Japonia a fost promovată cu un accent pe interesele comerciale în schimbul nevoilor de sănătate publică. Această situație nu este unică la nivel național și a fost observată în alte țări. În Australia, de exemplu, în ciuda îndoielilor considerablie ale Comitetului Consultativ al Beneficiilor Farmaceutice în privința vaccinului Gardasil, decizia comitetului de a respinge adăugarea Gardasil la programul național de vaccinare a fost deturnată în grabă, urmând interferenței politice si lobbyingului (60). În SUA, Merck & Co, Inc a promovat legislația mandatând vaccinarea HPV pentru școli servind ca o resursă informațională, făcînd lobby cu legiuitorii, redactând legislații, mobilizând femeile cu putere legislativă și organizațiile de medici, efectuând campaii de marketing, și ușurând accesul la vaccinuri. Legiuitorii s-au bazat pe Merck cu preponderență pentru informațiile științifice (61). Responsabilitatea dovedirii eficacității și siguranței vaccinului rămâne companiilor farmaceutice, iar guvernul este așteptat să monitorizeze și să ghideze aceste eforturi. Situația curentă în care interesele comerciale conduc politica guvernamentală trebuie corectată printr-o perspectivă a eticii medicale.
În prezent, Japonia este una dintre puținele țări în care recomandarea vaccinării HPV a fost temporar sistată; autoritățile de reglementare din alte țări nu și-au schimbat politica. Deși diverse grupuri de victime ale vaccinării au colaborat în activități pe scară largă, autoritățile de reglementare încă nu au admis relația de cauzalitate între vaccinuri și problemele de sănătate ale victimelor.
Decizia guvernului japonez de a înceta recomandarea vaccinului HPV, a încurajat într-o anumită măsură autoritățile de reglementare și pacienții din alte țări pentru a contesta valoarea vaccinului HPV. Este posibil ca eforturile Japoniei de a opri recomandarea să fi avut succes datorită influenței fondului istoric în privința cazurilor de poluare a mediului și a suferinței provocate de terapiile medicamentoase (de exemplu boala Minamata, talidomidă, SMOD, boala Creutzfeldt–Jakob, HIV transmis prin produse sanguine contaminate, etc.), ce au avut loc în perioada post-belică de accensiune economică rapidă. În procesele inentate, grupurile nu au cerut numai măsuri compensatorii, ci și reformă instituțională și revizuirea legii pentru a preveni repetarea acelorași greșeli (62).
Acest fond istoric a creat o situație în care mass-media și autoritățile de reglementare nu pot ignora cu ușurință plângerile vicimelor în legătură cu efectele secundare ale noilor vaccinuri. Aici putem găsi un indiciu în privința rezolvării acestei probleme. Este necesar să îmbrățișam transparența la fiecare pas al procesului de aprobare pentru produsele farmaceutice, de la dezvoltarea de noi medicamente, la supravegherea post-marketing. Simultan, este crucial să consolidăm rezolvarea conflictelor de interese, și să constituim un sistem prin care cetățenii să poată participa direct și să aibă o voce în planificarea politicii de sănătate publică (63, 64, 65).
Conflict de interese:
Toți autorii sunt membri ai Medwatcher Japan. Masumi Minaguchi și Masato Sekiguchi sunt avocați pentru reclamanții în procesele de vaccinare HPV.
Referințe
- Notificarea de la MHLW privind programul de vaccinare de rutină a vaccinului HPV 2013.6.14 [japoneză] [citat 2017 Mar 25]. Disponibil de la: http://www.mhlw.go.jp/stf/shingi2/0000091963.html
- Conferința internațională privind armonizarea cerințelor tehnice pentru înregistrarea medicamentelor de uz uman. ICH Orientarea armonizată tripartită Gestionarea datelor clinice de siguranță: definiții și standarde pentru raportarea rapidă E2A [citat 2017 Mar 25]. Disponibil la: https://www.imim.es/media/upload/arxius/MEDIA436.pdf
- Documentele 16 și 17 distribuite în cadrul reuniunii Consiliului Științelor în domeniul Sănătății, subcomisia de vaccinare, reuniunea grupului de lucru ADR, 23 mai 2016 [japoneză] [citat 2017 Mar 25]. Disponibil la: http://www.mhlw.go.jp/stf/shingi2/0000125164.html
- Documente distribuite la ședința Consiliului Științelor din domeniul Sănătății, subcomitetul de vaccinare, reuniunea grupului de lucru ADR, 12 aprilie 2016 [japoneză] [citat 2017 Mar 25]. Disponibil la: http://www.mhlw.go.jp/stf/shingi2/0000121045.html
- Documente distribuite la ședința Consiliului Științelor din domeniul sănătății, subcomitetul de vaccinare, reuniunea grupului de lucru ADR, 23 mai 2016 japoneză] [citat 2017 Mar 25]. Disponibil de la: http://www.mhlw.go.jp/stf/shingi2/0000125164.html
- Lawrence G, Aurul MS, Hill R, Deeks S, Glasswell A, McIntyre PB. Raport anual: Supravegherea evenimentelor adverse după imunizare în Australia, 2007. Commun Dis Intell Q Rep. 2008 Dec; 32 (4): 371-87.
- Centrul național de informare privind vaccinurile. Analiza efectuată de Centrul național de informare privind vaccinurile din rapoartele despre evenimentele adverse ale Gardasil & Menactra către sistemul de raportare a evenimentelor adverse pentru vaccinuri (VAERS), februarie 2009 [citat 2017 Mar 25]. Disponibil la: http://www.cbsnews.com/htdocs/NVICGardasilvsMenactraVAERSReportFeb2009.pdf
- Kinoshita T, Abe RT, Hineno A, Tsunekawa K, Nakane S, Ikeda S. Disfuncție nervoasă simptomatică periferică la fete japoneze adolescente după imunizarea cu vaccinul împotriva papilomavirusului uman. Intern Med. 2014; 53 (19): 2185-200.
- Yokota S, Kuroiwa Y, Nakamura I, Nakajima T, Nishioka K. Prezentare generală și discuție despre sindromul neuropatic asociat vaccinului HPV. Japonia Medical Journal (Nihon Iji Shimpou) 2015; 4758: 46-53 [japoneză].
- Hirai T, Kuroiwa Y, Hayashi T, Uchiyama M, Nakamura I, Yokota S, Nakajima T, Nishioka K, Iguchi Y. Efectele adverse ale vaccinării contra virusului papiloma uman asupra sistemului nervos central. Sistemul nervos autonom. 2016; 53: 49-64.
- Ikeda S. Complicații neurologice în vaccinarea cu HPV. Brain și nerv 2015; 67 (7): 835-43 [japoneză].
- Tomljenovic L, Shaw CA. Politica de vaccinare împotriva papilomavirusului uman (HPV) și medicamente bazate pe dovezi: sunt ele în contradicție? Ann Med. 2013 Mar; 45 (2): 182-93. Doi: 10.3109 / 07853890.2011.645353.
- Brinț L, Theibel AC, Pors K, Mehlsen J. Reacții adverse suspectate la vaccinul pentavalent de papilom uman. Dan Med J. 2015; 62 (4): A5064.
- Sfriso P, Ghirardello A, Botsios C, Tonon M, Zen M, Bassi N, Bassetto F, Doria A. Infecții și autoimunitate: relația multilaterală. J Leukoc Biol. Mar 2010; 87 (3): 385-95. Doi: 10.1189 / jlb.0709517. Epub 2009 Dec 16.
- Ratele de acoperire a imunizării în Japonia [citat 2017 Mar 25]. Disponibil la: http://www.mhlw.go.jp/topics/bcg/other/5.html
- Momentele Conferinței Consiliului Științelor în domeniul Sănătății, subcomitetul de vaccinare, reuniunea grupului de lucru ADR, 20 ianuarie 2014 [japoneză] [citat 2017 Mar 25]. Disponibil la: http://www.mhlw.go.jp/stf/shingi2/0000091998.html
- Comitetul consultativ global privind siguranța vaccinurilor: declarație privind siguranța vaccinurilor HPV, 17 decembrie 2015 [citată 2017 Mar 25]. Disponibil la: http://www.who.int/vaccine_safety/committee/GACVS_HPV_statement_17Dec2015.pdf?ua=1
- Reclamanții avocați ai proceselor HPV Vaccines Lawsuits [citat 2017 Mar 25]. Disponibil la: https://www.hpv-yakugai.net/
- Medwatcher Japonia. Prezentarea documentului “Refuzarea declarației GACVS (Comitetul consultativ global privind siguranța vaccinului) privind siguranța vaccinului împotriva HPV la 17 decembrie 2015”, noiembrie 2016 [citat 2017 Mar 25]. Disponibil la: http://www.yakugai.gr.jp/ro/topics/topic.php?id=930
- Takahata K, Takashima H. O propunere pentru un nou examen neurologic pentru discriminarea encefalopatiei autoimune și a tulburărilor somatoforme. Terapia neurologică. 2016; 33 (1): 9-18 [japoneză].
- Aratani S, Fujita H, Kuroiwa Y, Usui C, Yokota S, Nakamura I, Nishioka K, Nakajima T. Distrugerea hipotalamică murină cu apoptoză celulară vasculară după administrarea combinată a vaccinului împotriva virusului papiloma uman și a toxinei pertussis. Sci. Rep. 2016 Nov 11; 6: 36943. Doi: 10.1038 / srep36943.
- Nishioka K, Yokota S, Matsumoto Y. Caracteristicile clinice și criteriile preliminare de diagnostic ale vaccinării cu papilomavirus uman asociate cu sindromul neuroimunopatic (HANS). Int J Rheum Dis 2014; 17 (suppl 2): 6-29.
- Medwatcher Japan: Prezentarea unei solicitări de reconsiderare a regulilor privind conflictul de interese (COI) pentru consiliile Ministerului Sănătății, Muncii și Protecției Sociale – Având în vedere problemele legate de COI cu membrii consiliului privind vaccinurile HPV “, aprilie 2014 [citat 2017 Mar 25 ]. Disponibil la: http://www.yakugai.gr.jp/ro/topics/topic.
- Jefferson T, Jõrgensen L. Vaccinurile împotriva papilomavirusului uman, sindromul durerii regionale complexe, sindromul de tahicardie ortostatică posturală și disfuncția autonomă – revizuirea dovezilor de reglementare de la Agenția Europeană pentru Medicamente. Indian J Med Ethics 2017; 2 (1): 30-37.
- Gõtzsche PC, Jõrgensen KJ, MD, Jefferson T, Auken M, Brint L. Plângerea adresată Ombudsmanului European cu privire la administrarea defectuoasă la Agenția Europeană a Medicamentului (EMA) în legătură cu siguranța vaccinurilor HPV, 10 octombrie 2016 [citat 2017 Mar 25]. Disponibil la: http://nordic.cochrane.org/sites/nordic.cochrane.org/files/public/uploads/ResearchHighlights/Complaint-to-ombudsman-over-EMA.pdf
- Agenția Națională de Securitate a Medicamentului și a produselor de sănătate. Vaccinuri anti-HPV și riscurile maladiilor auto-imune: studiu farmaco-epidemiologic [franceză]. [Citat 2017 Mar 25]. Disponibil la: http://ansm.sante.fr/content/download/80841/1023043/version/1/file/Ansm_gardasil-Hpv2_Rapport_September-2015.pdf
- Rasmussen TA, Jõrgensen MR, Bjerrum S, Jensen-Fangel S, Stõvring H, õstergaard L, Sõgaard OS. Utilizarea ratelor de bază ale bolii bazate pe populație pentru evaluarea siguranței vaccinului în copilărie și imunizarea în masă în Danemarca: studiu de masă la nivel național. BMJ. 2012 Sep 17; 345: e5823. Doi: 10.1136 / bmj.e5823.
- Arnheim-Dahlström L, Pasternak B, Svanström H, Sparén P, Hviid A. Evenimente autoimune, neurologice și venoase tromboembolice după imunizarea fetelor adolescente cu vaccin pentavalent de papilomavirus uman în Danemarca și Suedia: studiu de masă. BMJ. 2013 Oct 9; 347: f5906. Doi: 10.1136 / bmj.f5906.
- Callréus T, Svanström H, Nielsen NM, Poulsen S, Valentiner-Branth P, Hviid A. Immunizarea papilomavirus umană a fetelor adolescente și raportarea anticipată a evenimentelor adverse mediate imun. Vaccin. 2009 14 mai; 27 (22): 2954-8. Doi: 10.1016 / j.vaccine.2009.02.106. Epub 2009 Mar 13.
- Descoperirea D, Hardt K, Spiessens B, Izurieta P, Verstraeten T, Breuer T, Dubin G.Protecția virusului papilomavirus uman (HPV) -16 / 18 Vaccinul cu adjuvant AS04 pentru prevenirea cancerului de col uterin: o analiză comună a 11 studii clinice. Hum Vaccin. 2009; 5 (5): 332-40.
- Chao C, NP Klein, Velicer CM, Sy LS, Slezak JM, Takhar H, Ackerson B, Cheetham TC, Hansen J, Deosaransingh K, Emery M, Liaw KL, Jacobsen SJ. Supravegherea stărilor autoimune după utilizarea de rutină a vaccinului tetravalent de papilomavirus uman. J Intern Med. 2012; 271 (2): 193-203.doi: 10.1111 / j.1365-2796.2011.02467.x. Epub 2011 15 noiembrie.
- Cusick MF, Libbey JE, Fujinam RS. Agitația moleculară ca mecanism al bolilor autoimune. Clin Rev Allergy Immunol. 2012; 42 (1): 102-11.
- Marson A, Housley WJ, Hafler DA. Baza genetică a autoimunității. J ClinInvest. 2015; 125 (6): 2234-41.
- Volkman, HE, Stetson DB. Inamicul: retroelemente endogene și boli autoimune. Nat Immunol. 2014; 15 (5): 415-22.
- Abbas AK, Lichtman AH, Pillai S. Toleranța imunologică și autoimunitatea. În: Abbas AK, Lichtman AH, Pillai S (eds). Cellular and Molecular Immunology, ed. Philadelphia: Elsevier Saunders; 2015, pp. 315-337.
- Castiblanco J, Anaya JM. Genetică și vaccinuri în era medicinii personalizate. Curr Genomics. 2015 Feb; 16 (1): 47-59. Doi: 10.2174 / 1389202916666141223220551.
- Healy D. Medicalizarea datelor. In: Pharmageddon. Berkeley și Los Angeles: Univ. Din California Press; 2012, pp.96-128.
- Herxheimer A. Farmacovigilența încă neglijează pacienții. Medicul prescris informat. 2014; 29 (5): 75-9 [japoneză].
- Einstein MH, Takacs P, Chatterjee A, Sperling RS, Chakhtoura N, Blatter MM, Lalezari J, David MP, Lin L, Struyf F, Dubin G; Grupul de studiu HPV-010 Comparație între imunogenitatea pe termen lung și siguranța vaccinului cu adjuvant vaccinat cu papilomavirus uman (HPV) -16 / 18 și a vaccinului HPV-6/11/16/18 la femei sănătoase cu vârsta cuprinsă între 18-45 ani: Din analiza unui studiu aleatoriu pentru faza III. Hum Vaccin Immunother. 2014; 10 (12): 3435-45. Doi: 10.4161 / hv.36121.
- Naud PS, Roteli-Martins CM, De Carvalho NS, Teixeira JC, de Borba PC, Sanchez N, Zahaf T, Catteau G, Geeraerts B, Descamps D. Eficacitatea susținută, imunogenitatea și siguranța HPV-16/18 AS04- Adjuvant vaccin: analiza finală a unui studiu de lungă durată de urmărire până la 9,4 ani după vaccinare. HumVaccin Immunother. 2014; 10 (8): 2147-62. Doi: 10.4161 / hv.29532.
- Asato T, Maehama T, Nagai Y, Kanazawa K, Uezato H, Kariya K. Un mare studiu de control al cazurilor de cancer de col uterin asociat cu infectia cu papilomavirus uman in Japonia, prin genotiparea secventierei nucleotidice. J Infect Dis. 2004 15 mai; 189 (10): 1829-32. Epub 2004 26 aprilie.
- Ho GY, Bierman R, Beardsley L, Chang CJ, Burk RD. Istoricul natural al infecției cu papilomavirus cervicovaginal la femeile tinere. N Engl J Med. 1998 Feb 12; 338 (7): 423-8.
- Woodman CB, Collins S, Winter H, Bailey A, Ellis J, Prior P, Yates M, Rollason TP, Young LS. Istoria naturală a infecției cu papilomavirus uman cervical la femei tinere: un studiu de masă longitudinal. Lancet. 2001; 357 (9271): 1831-6.
- Kawana K, Yasugi T. Papilomavirus uman și tulburare neoplazică. Antibiotice și chimioterapie. 2006; 22 (10): 1521-8 [în japoneză].
- Departamentul de vaccinuri și alte biologice. Stadiul actual al dezvoltării vaccinurilor profilactice împotriva infecției cu papilomavirus uman. Raportul unei întâlniri tehnice, Geneva, 16-18 februarie 1999.
- Paavonen J, Naud P, Salmeron J, Wheeler CM, Chow SN, Apter D, Kitchener H, Castellsague X, Teixeira JC, Skinner SR, Hedrick J, Jaisamrarn U, Limson G, Garland S, Szarewski A, Romanowski B, Aoki FY , Schwarz TF, Poppe WA, Bosch FX, Jenkins D, Hardt K, Zahaf T, Descamps D, Struyf F, Lehtinen M, Dubin G; Grupul de studiu HPV PATRICIA. Eficacitatea vaccinului cu HPV-16/18 cu adjuvant AS04 împotriva infecției cervicale și a precancerului cauzat de tipurile HPV oncogene (PATRICIA): analiza finală a unui studiu dublu-orb, randomizat, efectuat la femei tinere. Lancet. 2009; 374 (9686): 301-14. Doi: 10.1016 / S0140-6736 (09) 61248-4. Epub 2009 iulie 6.
- Quinn M, Babb P, Jones J, Allen E. Efectul screening-ului asupra incidenței și mortalității cauzate de cancerul colului uterin în Anglia: evaluarea bazată pe statistici colectate în mod obișnuit. BMJ. 1999; 318 (7188): 904-8.
- Actul imunizării [citat 2017 Mar 25]. Disponibil la: http://www.japaneselawtranslation.go.jp/law/detail/?id=2778&vm=04&re=01
- Consiliul de experți japonez pentru eradicarea cancerului de col uterin [citat 2017 Mar 25]. Disponibil de la: http://www.cczeropro.jp/
- Medwatcher Japonia. Plângerea împotriva încălcărilor presupuse ale producătorilor de vaccinuri HPV privind Codul de promovare al medicamentelor de prescripție JPMA [japoneză] [citat 2017 Mar 25]. Disponibil de la: http://www.yakugai.gr.jp/en/topics/topic.php?id=890
- Ghid de transparență pentru relația dintre activitățile corporațiilor și instituțiile medicale, Asociația producătorilor farmaceutici din Japonia (JPMA) [citată în 2017 Mar 25]. Disponibil la: http://www.jpma.or.jp/english/policies_guidelines/transparency_guideline.html
- Plângerea împotriva încălcărilor presupuse ale producătorilor de vaccinuri HPV privind Codul de Promovare al JPMA pentru medicamentele de prescripție [citat 2017 Mar 25]. Disponibil la: http://www.yakugai.gr.jp/en/topics/topic.php?id=890
- Recomandările de reformă anuale din partea Guvernului Statelor Unite la Guvernul Japoniei în cadrul inițiativei privind politica de reformă și de concurență din SUA-Japonia, 15 octombrie 2008 [citat 2017 Mar 25]. Disponibil la: https://ustr.gov/sites/default/files/uploads/agreements/morocco/pdfs/EHI%20USG%20Agenda%20Items%202-11-11%20FINAL.pdf
- Statele Unite ale Americii-JAPONIA. Inițiativa de Armonizare Economică, februarie 2011 [citată în 2017 Mar 25]. Disponibil la: https://www.google.com/url?q=https://ustr.gov/sites/default/files/2008-2009-Regul
- Wilson R, Paterson P, Larson HJ. Vaccinarea HPV în Japonia – probleme și opțiuni. CSIS, mai 2014 [citat 2017 Mar 25]. Disponibil de la: https://csis-prod.s3.amazonaws.com/s3fs-public/legacy_files/files/publication/140514_Wilson_HPVVaccination_Web.pdf
- Wilson R, Paterson P, Chiu J, Schulz W, Larson H. Vaccinarea HPV în Japonia – dezbaterea continuă și impactul global. CSIS, aprilie 2015 [citat 2017 Mar 25]. Disponibil la: https://csis-prod.s3.amazonaws.com/s3fs-public/legacy_files/files/publication/150422_Wilson_HPVVaccination2_Web.pdf
- Sheldon Krimsky. Știință în interesul privat: a ademenit profiturile corupte în cercetarea biomedicală? Oxford: Rowman & Littlefield Publishers, Inc; 2003, p4.
- Heath I. În urma povestirii: continuitatea îngrijirii în practica generală. În: Greenhalgh T, Hurwitz B (eds). Medicament bazat pe narrație. Londra: cărți BMJ; 1998, p. 86.
- Rudebeck CE. Umanismul în medicină. Benevolent sau realism? Scand J Prim Sănătate. 1992 Sep; 10 (3): 161-2.
- Hart E. Istoricul vaccinării globale rapide și controversate cu HPV [citat 2017 Mar 25]. Disponibil la: https://elizabethhart.files.wordpress.com/2013/02/the-history-of-questionable-fast-trackedglobal-hpv-vaccination.pdf
- Mello MM, Abiola S, Colgrove J. Rolul companiilor farmaceutice în elaborarea politicilor de vaccinare de către stat: cazul vaccinării cu vaccin umanpapillomavirus. Am J Sănătate publică. 2012 Mai, 102 (5): 893-8. Doi: 10.2105 / AJPH.2011.300576. Epub 2012 Mar 15.
- Suzuki T, Minaguchi M, Sekiguchi M. Legea și siguranța drogurilor. Institutul Eidell; 2015, p.348 [japoneză].
- Chalmers I. Ce vreau de la cercetare în domeniul sănătății și cercetători când sunt pacient? BMJ. 1995; 310 (6990): 1315-1318.
- Doshi P, Dickersin K, Healy D, Vedula SS, Jefferson T. Restaurarea studiilor invizibile și abandonate: un apel pentru publicarea rezultatelor. BMJ. 2013 iunie 13; 346: f2865. Doi: 10.1136 / bmj.f2865.
- Beppu H. Motive pentru care pacienții trebuie să participe la planificarea studiilor clinice. The Informed Prescriber 2010; 25 (4): 45-9 [Japoneză].
Reclame
Citiți vă rog și:
- VACCINAT vs. NEVACCINAT: Cine e MAI BOLNAV ? STUDIU INEDIT efectuat pe COPII americani VACCINAȚI, comparativ cu COPII NEVACCINAȚI
-
O fetiță de 12 ani dezvoltă sindrom Guillain-Barré după VACCINUL GARDASIL și suferă de PARALIZIE
- BIG PHARMA creaza medicamente. Apoi inventeaza boli pentru acele medicamente …
Ne străduim să menținem viu acest site și să vă punem la dispoziție informații care să facă lumină în provocările pe care le trăim. Activitatea independentă a OrtodoxINFO funcționează strict cu ajutorul cititorilor, din acest motiv vă cerem acum ajutorul. Ne puteți sprijini printr-o donație bancară sau prin PayPal, completând formularul de mai jos.
Mulțumim celor care ne-au ajutat până acum!




